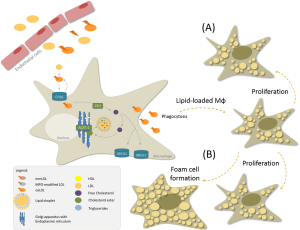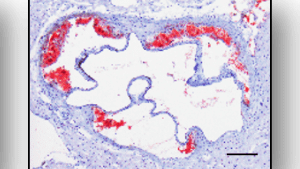
Prozess der Schaumzellbildung durch oxidiertes LDL
Foto: Maria Wallertα-TOH - Neue Behandlungsstrategien für Atherosklerose-induzierte Komplikationen – Schlaganfall und Myokardinfarkt
Atherosklerose-induzierte Komplikationen, wie z.B. Myokardinfarkt und Schlaganfall gehören zu den führenden Todesursachen weltweit. Daher sind neue Behandlungsmöglichkeiten zwingend notwendig. Ein enormer Fortschritt in der Behandlung war die Einführung der frühen Reperfusion des betroffenen ischämischen Gewebes. Paradoxer Weise führt jedoch genau diese Behandlung zu einem verstärkten entzündungs- und oxidativen Stress-induzierten Zelltod, und damit zu einer dramatischen Schädigung des betroffenen Gewebes (Herzens/Gehirns), dem sogenannten Ischämie/Reperfusionsschaden. Vitamin E ist bekannt für seine anti-oxidativen und anti-inflammatorischen Eigenschaften. Daher haben wir untersucht, in wie fern Vitamin E den oxidative und inflammatorischen Stress im Ischämie/Reperfusionsschädigungsmodell reduziert, und damit die Herzfunktion erhält bzw. wiederherstellt. Ziel dieser Studie soll es sein, die Relevanz von Vitamin E in der Therapie von Myokardinfarkt und Schlaganfall einzuschätzen.
Effekte von LCMs in der Atherosklerose – Plaquebildung und -Stabilität
Aufgrund der bekannten Wechselwirkungen von Vitamin E mit Entzündungsprozessen und der Schaumzellbildung, welche in in-vitro Studien überzeugend gezeigt werden konnten, wurde eine anti-atherogene Wirkung von Vitamin E postuliert. Bisher ist es jedoch nicht gelungen eindeutige protektive Effekte von Vitamin E auf kardiovaskuläre Ereignisse in randomisierten, kontrollierten Humanstudien (randomised controled trials, RCTs) zu zeigen. Neueste Studien konzentrieren sich auf die Wirkung der langkettigen Vitamin E-Metabolite (LCMs), welche in der Leber durch den Metabolismus von Vitamin E gebildet werden. Bisher konnte gezeigt werden, dass besonders die Metabolite des α-Tocopherols (α-TOH), α-LCMs, hoch potent inflammatorische Reaktionen hemmen und den Lipidmetabolismus regulieren. Dabei ist zu beobachten, dass die Effekte der LCMs teilweise über andere Signalwege vermittelt werden, als vom α-TOH bekannt. Daher gehen wir davon aus, das den LCMs eine größere Bedeutung zukommt, als bisher vermutet. Weiterführend stellen wir die These auf, dass die teils kontroversen Ergebnisse zu protektiven Effekten des α-TOH auf die Atherogenese bzw. kardiovaskuläre Ereignisse aus der individuell unterschiedlichen Metabolisierung und damit einhergehend der Bildung der LCMs einhergeht. Basierend auf den bisherigen Daten vermuten wir, dass α-LCMs die Progression der Atherosklerose beeinflussen. Dabei gehen wir davon aus, dass Effekte abhängig von der Struktur genauer der endständigen Oxidation der Seitenkette konzentrationsabhängig vermittelt werden. Für die Verifizierung dieser Hypothese wurde die Wirkung der α-LCMs im Vergleich zu α-TOH auf atherogene Prozesse, wie die Entstehung der stabilen und instabilen Plaques in etablierten Tiermodellen untersucht. Sofern diese Studien eine anti-atherogene Wirkung der getesteten Verbindungen aufzeigen, könnten diese als Leitsubstanzen neuer Medikamente in der Therapie von Atherosklerose dienen.
Einfluss von LCMs auf die Entzündungsantwort von Immunzellen
Überschießende Entzündungs- (inflammatorische) Reaktionen sind zentrale Ereignisse altersassoziierter Erkrankungen, wie beispielsweise der Atherosklerose und des Diabetes mellitus type II sowie damit einhergehenden Komplikationen. Es ist bekannt, dass Vitamin E ursprünglich beschrieben als Antioxidans zusätzliche anti-inflammatorische Effekte vermittelt. Die Wirkung der metabolischen Abbauprodukte von Vitamin E, LCMs, auf akute und chronische Entzündungsprozesse sind hingegen nur unvollständig untersucht. Bisherige Untersuchungen unserer Arbeitsgruppe zeigen ein ausgeprägtes anti-inflammatorisches Potential der LCMs in Lipopolysaccharid (LPS)-induzierten Mausmakrophagen auf Gen- und Proteinexpression sowie auf funktionaler Ebene. Die Effekte der LCMs werden dabei teilweise über α-TOH-unabhängige Signalwege vermittelt. Dieses Teilprojekt verfolgt daher das langfristige Ziel die ganzheitliche Wirksamkeit der physiologisch-relevanten LCMs auf die Antwort von Entzündungsreaktionen in in-vitro und in in-vivo Testsystemen zu untersuchen um den Einfluss der LCMs in entzündungsgetriebenen Erkrankungen besser beurteilen zu können. Dabei steht im Fokus die Wirksamkeit der LCMs von denen des α-TOH abgrenzen zu können und den Effekten zugrundeliegenden Signalwegen aufzuklären.