Rezeptoridentifikation
Wie erkennen Zellen langkettige Vitamin E-Metabolite?
Vitamin E ist ein wichtiges fettlösliches Antioxidans, das u.a. zur Prävention altersbedingter Erkrankungen eingesetzt wird. Allerdings zeigen Metaanalysen zur Wirksamkeit von Vitamin E in der Behandlung verschiedener Krankheiten widersprüchliche Ergebnisse. Daher wird der therapeutische Effekt einer Vitamin E-Gabe kontrovers diskutiert. Ein tiefgreifendes Verständnis der biologischen Aktivität und des Metabolismus von Vitamin E ist daher zwingend notwendig, um die Wirksamkeit einschätzen zu können. Neueste Studien legen nahe, dass die Gabe von α-Tocopherol (wichtigste Form von Vitamin E; Abkürzung α-TOH) die zelluläre Signalweiterleitung sowie die Expression von Genen, die an Inflammation, Proliferation, Lipidmetabolismus und anderen zellulären Prozessen beteiligt sind, beeinflusst. Während des Metabolismus von Vitamin E werden die langkettigen Metabolite (engl. long-chain metabolites; Abkürzung LCM) 13′-hydroxychromanol (13′-OH) and 13′-carboxychromanol (13′-COOH) durch oxidative Modifikation der Seitenkette gebildet. Der Nachweis dieser Metabolite im menschlichen Blutserum deutet dabei auf ihre physiologische Relevanz hin. Es wurden bereits Effekte der LCM auf den Lipidmetabolismus, die Apoptose, die Proliferation und entzündliche Prozesse sowie den Tocopherol- und Fremdstoffmetabolismus gezeigt. Daher könnte die metabolische Aktivierung von α-TOH (d.h. die Bildung der langkettigen Metabolite) die beobachteten Effekte nach α-TOH-Gabe erklären. Das Ziel dieses Teilprojektes ist es, LCM-spezifische Rezeptoren, die deren regulatorische Funktionen weiterleiten, zu identifizieren und zu charakterisieren.
Modulation adaptiver Stressantworten
Fördern langkettige Vitamin E-Metabolite zelluläre Schutzmechanismen?
„Alle Dinge sind Gift, und nichts ist ohne Gift; allein die Dosis machts, dass ein Ding kein Gift sei.“ Diese Paracelsus zugeschriebene Maxime ist ein Grundprinzip der Toxikologie und zudem die Basis für die Prinzipien der „Hormesis“ bzw. adaptiven (zellulären) Stressantwort. „Hormesis“ beschreibt eine dosisabhängige Antwort auf eine Umweltsubstanz in zwei Phasen. Phase 1 ist charakterisiert durch einen positiven Effekt bei niedriger Dosis und Phase 2 durch einen inhibitorischen oder toxischen Effekt bei zu hoher Dosis. Die weithin bekannten positiven Effekte von sportlicher Aktivität werden als ein Beispiel für erwünschte Wirkungen durch hormetische Effekte betrachtet. Der milde Stress durch die physische Aktivität führt zu Anpassungsmechanismen des muskuloskeletalen und kardiovaskulären Systems. Diese Anpassung vermittelt eine erhöhte Resistenz dieser Systeme gegen Verletzungen und Krankheiten. Die langkettigen Vitamin E-Metabolite (LCM) zeigen zytotoxische Effekte in hohen Dosierungen in zellulären Systemen, aber positive regulatorische Funktionen bei niedriger Dosierung. Das Ziel dieses Projektes ist die Charakterisierung des durch die LCM ausgelösten Stresses und der zellulären Anpassungsmechanismen. Weiterhin soll geklärt werden, ob die Modulation zellulärer Entgiftungsmechanismen und die Anpassung an den Stress durch LCM einen Schutz gegen gesundheitsschädliche Substanzen oder in pathologischen Zuständen vermitteln kann.
Einfluss der LCM auf die Entzündungsantwort
Wie schützen die langkettigen Vitamin-E-Metabolite vor überschießenden Entzündungsreaktionen?
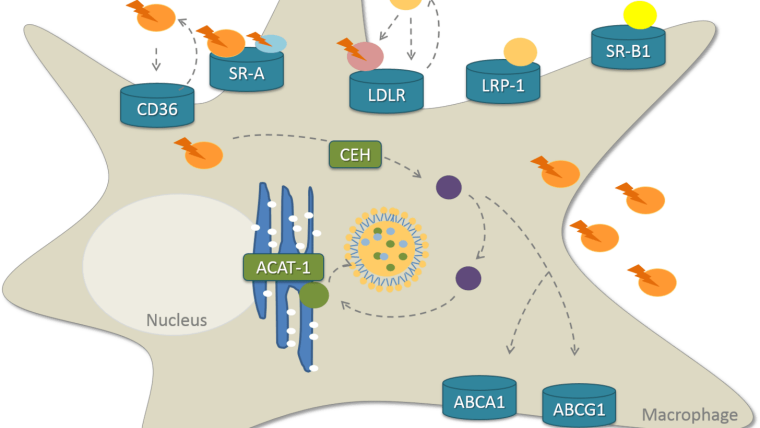
Entzündungen sind die treibende Kraft hinter vielen altersbedingten Erkrankungen wie Atherosklerose und Diabetes mellitus Typ II. Neben ihren Effekten als Antioxidantien wurden Vitamin E-Formen auch als anti-inflammatorische Substanzen beschrieben. Allerdings ist wenig darüber bekannt, wie genau verschiedene Vitamin E-Formen unter akuten und chronischen entzündlichen Bedingungen wirken. Wir wissen heute, dass die LCM beispielsweise potente anti-inflammatorische Verbindungen sind, die pro-inflammatorische Mechanismen zum Teil anders beeinflussen als ihre Vorläufer-Substanz (α-TOH). Beispielsweise verändern die LCM die Inflammationsantwort von stimulierten Mausmakrophagen auf Gen-, Protein- und funktioneller Ebene in positiver Weise. Das Ziel dieses Projektes ist es, den Einfluss der physiologisch relevanten LCM auf die Entzündungsantwort näher zu untersuchen. Von besonderem Interesse sind dabei die zu Grunde liegenden Signalwege, über die die LCM anti-inflammatorische Effekte in vitro und in vivo vermitteln.